Amadeo Avogadro olasz tudós 1811-ben publikálta hipotézisét, melyet csak közel 50 évvel később fogadott el a tudóstársadalom, és kezdték Avogadro-törvénye (tétele) néven emlegetni. Ez a következőt mondja ki:
Fontos, hogy az Avogadro-törvényben a gázrészecskék (gázmolekulák) darabszáma szerepel, nem pedig az atomok darabszáma. (Az atom és a molekula fogalma csak az Avogadro-hipotézissel vált szét.)
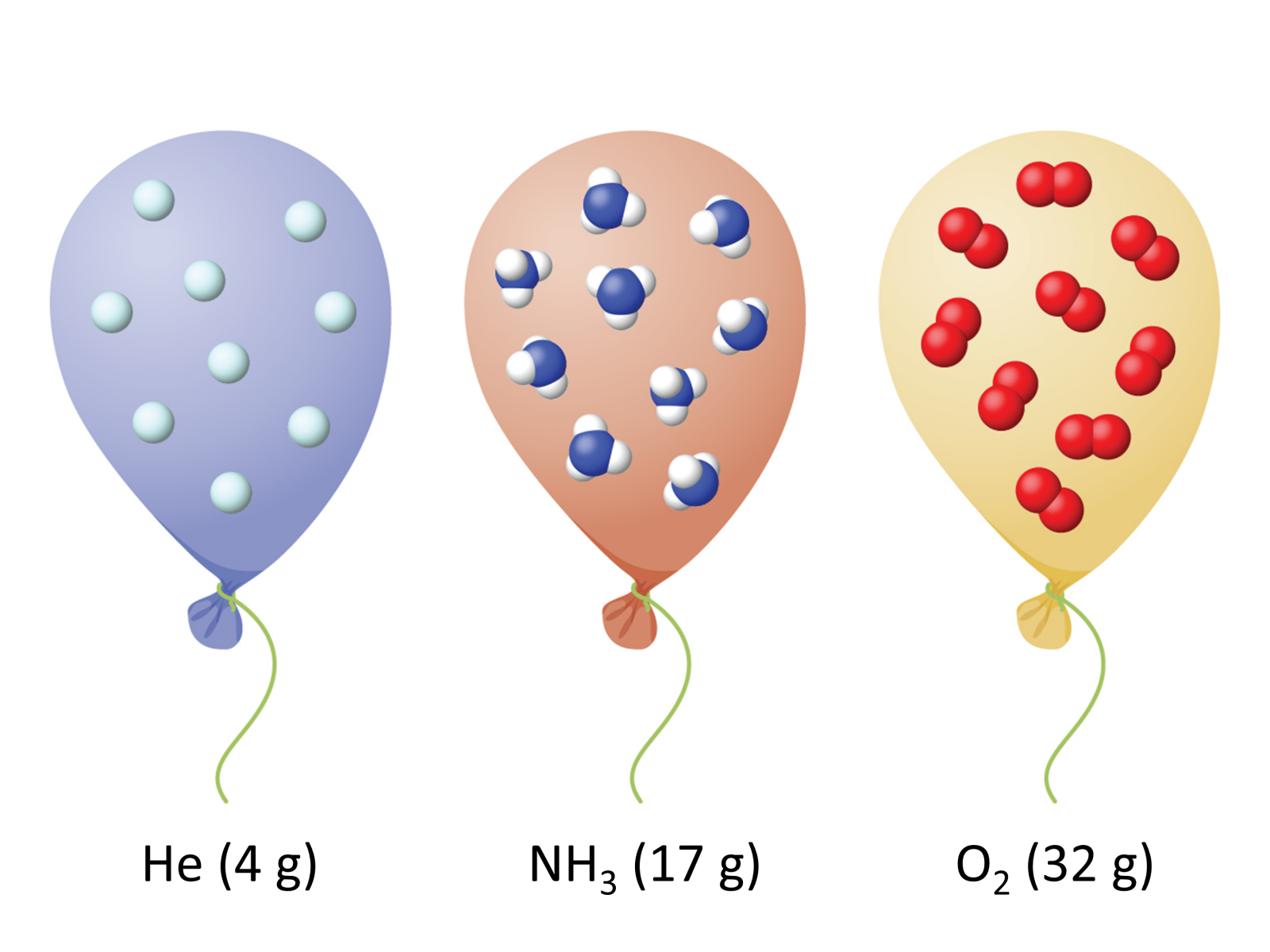
Az alábbi ábra azt szemlélteti, ha mondjuk van három azonos méretű \((24,5\ \mathrm{literes})\) lufink, mindegyikben \(25\ \mathrm{{}^\circ C}\) a hőmérséklet és \(101\ 325\ \mathrm{Pa}\) a nyomás, akkor mindhárom lufiban ugyanannyi (\(6\cdot 10^{23}\ \mathrm{db}\)) gázmolekula van, pedig ha az egyik hidrogént tartalmaz, akkor abban a gáz tömege csak \(4\ \mathrm{g}\), az ammóniával töltöttben már \(17\ \mathrm{g}\), az oxigénnel töltöttben pedig \(32\ \mathrm{g}\). Vegyük észre, hogy az azonos állapotú gázokban lévő atomok száma nem azonos, hanem a gázmolekulák száma egyezik meg a három lufiban! A héliumgáz egyatomos molekulákból áll, míg az ammóniagáz négyatomos, az oxigéngáz pedig kétatomos molekulákat tartalmaz.
A törvény állításán még 200 évvel felfedezése után is merjünk meglepődni! Hiszen a különböző fajtájú gázok molekuláinak sok tulajdonsága igen eltérő: a molekulák tömegei, a molekulák méretei és a sebességeik is. Például ha a legkisebb és legnagyobb rendszámú nemesgázt összehasonlítjuk:
| \(\mathrm{He}\) (hélium) | \(\mathrm{Rn}\) (radon) | ||
| atom- tömegek | értékei $(\mathrm{u})$ | 4 | 222 |
| aránya | \(1:55,5\) | ||
| atom- sugarak | értékei $(\mathrm{pm})$ | 31 | 200 |
| aránya | \(1:6,45\) | ||
| molekula- sebességek (átlagos, \(0\ \mathrm{^\circ C}\)) | nagyságai \(\left(\displaystyle \mathrm{\frac{m}{s}}\right)\) | 1304 | 175 |
| aránya | \(7,5:1\) | ||
Tehát hiába van sokszoros különbség az egyes gázfajták molekuláinak tömege, mérete, sebessége között (még azonos nyomáson és hőmérsékleten is), a gázmolekulák térbeli sűrűsége mégis azonos. (Mármint "az egységnyi térfogatban lévő molekulák darabszáma" értelmű térbeli sűrűség, nem pedig a "sűrűség", ami alatt leggyakrabban a $\varrho$ tömegsűrűséget értjük, ami pedig az egységnyi térfogatban lévő anyag tömegét jelenti). Szemléletesen úgy képzeljük, hogy ha egy-egy molnyi kétféle gázból az egyik gáz nagyobb méretű molekulákból áll, akkor az nagyobb tárfogatot is "tölt be". Az Avogadro-törvény pont az mondja, hogy bármilyen furcsa is számzunkra, de azonos lesz a két gáz térfogata (ha a hőmérsékleteik és nyomásaik azonos).
Az Avogadro-törvény érvényessége
Avogadro törvénye nem egzakt természettörvény, hanem egy kisebb-nagyobb pontossággal helytállónak bizonyult állítás. Egy gázra annál nagyobb pontossággal érvényes az Avogadro-tétel, minél nagyobb pontossággal teljesíti az ideális gáz kritériumait, vagyis hogy a gázmolekulák sokkal nagyobb térfogatot töltenek be, mint amennyi a gázmolekulák saját terfogatainak összege, és a mozgási energiájuk sokkal nagyobb, mint amekkora a két molekula közötti másodlagos erő potenciális energiája (szemléletesen: a gáz minél inkább ritka és forró). Az Avogadro-hipotézis a fenomenologikus (jelenségalapú, nem pedig a belső szerkezet elemzésén alapuló) gáztörvények sugalmazására intuitív módon született feltevés, melyet jóval később, a kinetikus gázelméletben az ideális gázokra sikerült levezetni is.
Az \(N_{\mathrm{A}}\) Avogadro-állandó
Az $N_{\mathrm{A}}$ Avogadro-állandó (más néven Avogadro-konstans) definíció szerint 1 molnyi anyagmennyiségű rendszerben lévő részecskék darabszáma:
\[N_{\mathrm{A}}=\frac{N}{n}\]
vagy másképp felírva
\[N=N_{\mathrm{A}}\cdot n\]
ahol $n$ a anyagmennyiséget ("mólszámot"), $N$ a részecskeszámot jelöli. Fontos, hogy az anyagmennyiség illetve a részecskeszám megadásánál mindig meg kell adni azt is, hogy mit tekintünk részecskének: egy molekulát, atomot, iont stb.
Ehhez azonban először definiálnunk kell a mól fogalmát. A \(\mathrm{mol}\) 2019-ben született (bár a legtöbb országban még ratifikálás és kihirdetés előtt álló) legújabb definíciója:
\(1\ \mathrm{mol}\) az anyagmennyisége egy rendszernek, melyben pontosan \(6,02217046\cdot 10^{23}\ \mathrm{db}\) részecske található.
A részecske ("entitás") lehet atom, molekula, ion, elektron stb. (1971. és 2019. között a mól definíciója úgy szólt, hogy \(1\ \mathrm{mol}\) az anyagmennyisége \(12\ \mathrm{gramm}\) tömegű \(\mathrm{^{12}C}\) szénnek, azaz 12-es tömegszámú szénnek.)
Abból adódóan, hogy az \(n\) anyagmennyiségnek van mértékegysége, a \(\mathrm{mol}\), ellentétben az \(N\) részecskeszámmal, aminek nincs:
\[[n]=\mathrm{mol}\]
\[[N]=1\]
következik, hogy az Avogadro-konstans is rendelkezik mértékegységgel:
\[[N_{\mathrm{A}}]=\frac{[N]}{[n]}\]
\[[N_{\mathrm{A}}]=\mathrm{\frac{1}{mol}}\]
Az Avogadro-konstans számértéke önkényesen meghatározott (bár a korábbi definícióból adódó legpontosabb értékhez igazították). Az Avogadro-állandót nem helyes Avogadro-számnak nevezni, mert ez az elnevezés azt sugallja, mintha ez csak egy (mértékegység nélküli)) szám lenne, márpedig az Avogadro-konstansnak van mértékegysége, az \(\displaystyle \mathrm{\frac{1}{mol}}\). Az "Avogadro-szám" a 19. században volt használatos fogalom. Egyébként az Avogadro-konstans számértéke nagyjából azonos \(1\ \mathrm{gramm}\) tömegű \(^1\mathrm{H}\) hidrogénben található atomok számával.
Gázok moláris térfogata (normál és standard "állapot"-ban)
Az Avogadro-törvény alapján adott nyomás, hőmérséklet és anyagmennyiség esetén minden (ideálisnak tekinthető) gáz azonos térfogatú. A két gyakori esetben (a normál állapotban illetve a standard más néven sztenderd állapotban) az egységnyi anyagmennyiségű (1 mol) gázok térfogatát az alábbi táblázat mutatja, melynek eredete az ideális gázok állapotegyenlete:
\[p\cdot V=n\cdot R\cdot T\]
$T$ hőmérséklet | \(p\) nyomás | $V_m$ moláris gáztérfogat \(\left(n=1\ \mathrm{mol}\right)\) | |
| normál állapot | \(\mathrm{0\ {}^\circ C}\) | \(101\ 325\ \mathrm{Pa}\) | \(22,41\ \mathrm{dm^3}\) |
| standard állapot | \(25\ \mathrm{{}^\circ C}\) | \(101\ 325\ \mathrm{Pa}\) | \(24,5\ \mathrm{dm^3}\) |
A standard és normál állapot fogalmakat eltérően használják a világ országaiban. Régebben sok országban nemcsak a hőmérsékletet határozták meg ezek a fogalmak, hanem a nyomást is, méghozzá \(101\ 325\ \mathrm{Pa}\)-ban. Ekkor vésődött be a fejekbe és a könyvekbe, táblázatokba, hogy a normál állapotú gázok moláris térfogata \(22,41\ \mathrm{dm^3}\), a standard pedig \(24,5\ \mathrm{dm^3}\). Aztán a IUPAC (International Union of Pure and Applied Chemistry azaz Nemzetközi Elméleti és Alkalmazott Kémiai Szövetség) hiába vezette be (1982-ben) a jelenleg is érvényes definíciót, miszerint a gázok standard állapota esetén a nyomás nem \(101\ 325\ \mathrm{Pa}\), hanem kerek \(100\ 000\ \mathrm{Pa}\) (ami pont \(1\ \mathrm{bar}\)), ez a módosítás nem terjedt el, nem ment át a gyakorlatba. A jelenlegi IUPAC definíció szerinti standard moláris gáztérfogat \(24,788\ \mathrm{liter}\). A IUPAC rendszerében egyébként a "normál állapot" fogalma nem is szerepel, hanem a "normál" jelző csupán annyit jelent, hogy a nyomás \(101\ 325\ \mathrm{Pa}\) értékű (amivel \(0\ \mathrm{{}^\circ C}\) hőmérsékleten ki is jön a megszokott \(22,41\ \mathrm{liter}\) a "normál moláris gáztérfogatra").
Az Avogadro-törvény egy következménye: a gázok sűrűsége
Az Avogadro-törvény alapján adott nyomáson, hőmérsékleten és térfogaton a nagyobb tömegű molekulákból álló gáz össztömege nagyobb, hiszen azonosak a molekulaszámok. Pontosabban fogalmazva: a különféle gázok \(m\) tömegei a \(\mu\) molekulatömegeikkel egyenesen arányosak:
\[\frac{m_1}{\mu_1}=\frac{m_2}{\mu_2}=\mathrm{konst.}\]
Ha a különféle gázok tömege egyenesen arányos a molekulatömeggel, akkor a gázok sűrűsége, ami
\[\varrho =\frac{m}{V}\]
az is arányos a molekulatömeggel:
\[\frac{\varrho_1}{\mu_1}=\frac{\varrho_2}{\mu_2}=\mathrm{konst.}\]
Tehát a nagyobb molekulatömegű gázoknak a sűrűsege is nagyobb (azonos hőmérséklet és nyomás esetén). De mi nem szoktuk tudni a gázok molekuláinak tömegét, viszont a gázok $M$ moláris tömegeit igen. Nézzük meg, hogyan függenek össze a különféle gázok sűrűségei a moláris tömegeikkel! Egy gáz \(M\) moláris tömege megkapható, ha az \(\mu\) molekulatömeget megszorozzuk az \(N_{\mathrm{A}}\) Avogadro-állandóval:
\[M=\mu \cdot N_{\mathrm{A}}\]
ebből kifejezve a molekulatömeget:
\[\mu=\frac{M}{N_{\mathrm{A}}}\]
Írjuk be ezt az előző, sűrűséges egyenletünkbe:
\[\frac{\varrho_1}{\mu_1}=\frac{\varrho_2}{\mu_2}=\mathrm{konst.}\]
\[\frac{\varrho_1}{\displaystyle \frac{M_1}{N_{\mathrm{A}}}}=\frac{\varrho_2}{\displaystyle \frac{M_2}{N_{\mathrm{A}}}}=\mathrm{konst.}\]
\[\varrho_1\cdot \frac{N_{\mathrm{A}}}{M_1}=\varrho_2\cdot \frac{N_{\mathrm{A}}}{M_2}=\mathrm{konst.}\]
ahol ha az \(N_{\mathrm{A}}\) Avogadro-állandóval egyszerűsítünk, akkor azt kapjuk, hogy:
\[\frac{\varrho_1}{M_1}=\frac{\varrho_2}{M_2}=\mathrm{konst.}\]
ahol persze a jobb oldali konstans már nem ugyanaz, mint ami az előző sorban szerepelt, de hát az egyenes arányosság szempontjából mindegy, hogy pontosan mekkora a konstans, elég, hogy a hányadosok értéke mindig azonos.
Vagyis a gázok sűrűsége is arányos a moláris tömeggel. Tehát a különféle gázok sűrűséggel kapcsolatos viselkedése pusztán a moláris tömegeik alapján megjósolható: a nagyobb moláris tömegű gáz (a nagyobb sűrűsége miatt) lesüllyed, a kisebb moláris tömegű pedig felszáll (ha más effektusok nem írják ezt felül). Nézzük ennek pár esetét a mindennapokból!
A borospincékben a kipréselt szőlőlé erjedése során \(\mathrm{CO_2}\) szén-dioxid gáz keletkezik, aminek a moláris tömege \(\left(\displaystyle 44\ \mathrm{\frac{g}{mol}}\right)\) nagyobb, mint a levegőé \(\left(\displaystyle 29\ \mathrm{\frac{g}{mol}}\right)\). Emiatt a termelődő szén-dioxid gáz leszáll, és a pince alján összegyűlve egy réteget alkot (mintha valami folyadék lenne). A szén-dioxid belélegzése eszméletvesztést okoz, amitől az elájult, elesett ember orra a pince legaljára kerül, ahol a legnagyobb a szén-dioxid koncentráció, így esélye sincs magához térni, segítséget hívni. Ezt megelőzendő szoktak a borászok a lépcsőn lefelé menet gyertyát égetni maguk előtt derékmagasságban: ha a gyertya kialszik, akkor alulról felgyűlt az erjedéskor keletkezett szén-dioxid.

Emiatt lehet a szén-dioxid gázt szinte önteni egy edényből, mintha folyadék lenne. Ha egy edényben szódabikarbóna és ecet összeöntésével szén-dioxidot feljesztünk, akkor azt "ráönthetjük" egy gyertyára, ami attól egyből elalszik:

A mélygarázsokba ugyanilyen okoból nem szabad LPG (Liquified Petroleum Gas, ami kb. $40\%$ propánból és $60\%$ butánból áll) autógázzal működő járművel behajtani, mert egy esetlegesen szivárgáskor a \(44\) illetve \(\displaystyle 58\ \mathrm{\frac{g}{mol}}\) moláris tömegű propán és bután felgyűlik, és robbanásveszélyes gázelegy jöhet létre.
Emiatt szállnak lefelé az öngyújtógázzal (bután) felfújt szappanbuborékok, míg a földgázzal (\(\mathrm{CH_4}\) metán) felfújtak felszállnak, ahogy a csupán \(\displaystyle 4\ \mathrm{\frac{g}{mol}}\) moláris tömegű héliummal töltött lufik is, ha nem rakunk annyi terhelést rájuk, hogy épp lebegjenek:
Vagy a \(\displaystyle 2\ \mathrm{\frac{g}{mol}}\) moláris tömegű hidrogéngázzal töltött Zeppelin léghajók is emiatt emelekdtek a magasba (csak a hidrogén éghető gáz, ezért nemcsak lassúnak, széljárásfüggőnek, de életveszélyesnek is bizonyult, ezért hamarosan eltűnt). Éghetetlen héliumra azért nem lehetett lecserélni a hidrogént, mert az elképesztően drága.
Ezzel szemben a hőlégballonban lévő gáz a molekulatömegek miatt kisebb sűrűségű a levegőnél, hanem mert azonos nyomáson magasabb hőmérsékletű:
Gyakori tévedések az Avogadro-törvénnyel kapcsolatban
Sokan (tévesen) azt az állítást gondolják Avogadro-törvénynek, hogy "a gázok moláris térfogata normál állapotban \(22,41\ \mathrm{liter}\)", illetve hogy "a gázok moláris térfogata standard állapoban \(24,5\ \mathrm{liter}\)".
Másik gyakori - szintén hibás - elképzelés, miszerint Avogadro-törvénye azt mondaná ki, hogy állandó nyomáson és hőmérsékleten egy adott gáz térfogata és mólszáma egyenesen arányos:
Ez utóbbi állítás - ha kicsit is belegondolunk - teljesen nyilvánvaló, ezért alaptalan dolog lenne törvényként felfogni. Hiszen ha egy tartályban lévő gázt ketté választunk (egy válaszfal behelyezésével), akkor a tartály egyik felének térfogata az eredeti térfogat felével egyeznek meg, és nyilvánvaló, hogy a benne lévő molekulák száma is a kezdeti molekulaszám fele lesz.
A térfogat és a mólszám egyenes arányossága akkor mutatja Avogadro törvényét, ha kihangsúlyozzok, hogy bármilyen gáz esetében ugyanakkora értékű a térfogat és a mólszám hányadosából adódó arányossági tényező, azonos nyomás és hőmérséklet esetén:
\[\frac{V_1}{n_1}=\frac{V_2}{n_2}=\mathrm{konst.}\]
\[(\mathrm{azonos}\ T\ \mathrm{és}\ p\ \mathrm{esetén\ minden\ gázra})\]
A gyakori - hibás - interpretációkban azonban adott gázról szokták mondani, hogy a térfogata és mólszáma állandó, ami csupán egy trivialitás.
Az Avogadro-állandó kapcsolata más fizikai állandókkal
Az $R$ univerzális gázállandó és a $k_{\mathrm{B}}$ Boltzmann-állandóval (amit sokszor csak egyszerűen $k$ betűvel jelölünk):
\[R=k_{\mathrm{B}}\cdot N_{\mathrm{A}}\]
Az $F$ Faraday-állandó és az $e$ elemi töltés között pedig fennáll:
\[F=N_{\mathrm{A}}\cdot e\]
Az Avogadro-állandó, az \(u\) atomi tömegegység (atomic mass unit, más néven \(\mathrm{dalton}\), ami egy \(^{12}\mathrm{C}\) atom tömegének \(\displaystyle \frac{1}{12}\)-ed része; \(u=1,66053904\cdot 10^{-27}\ \mathrm{kg}\)) valamint a szén \(M_{\mathrm{C}}\) moláris tömegének kapcsolata:
\[M_{\mathrm{C}}=12\cdot u\cdot N_{\mathrm{A}}\]
Az Avogadro-konstans meghatározása méréssel
Az \(N_{\mathrm{A}}\) meghatározása méréssel nem könnyű feladat, és 2019. előtt bő 100 éven át szép kihívást jelentett a kísérleti fizikusoknak, mire az új mol-definíció okafogyottá tette a kísérleti meghatározását. Számos közvetlen és közvetett módszerrel történt mérés, csak említés szintjén ezekből néhány:
- Brown-mozgás alapján: egyetlen kolloid részecskének az eredeti helytől adott idő alatt történő x irányú eltávolodásainak mikroszkóppal történő megfigyelésével
- Ülepedés vizsgálatával: folyadékban lévő kolloid részecskék (szuszpenzió) sűrűségeloszlását a magasság függvényében meghatározva; a mikroszkóp látómezejében lévő kolloid részecskék darabszámának megszámolásával
- Stokes-törvény alapján: súrlódó közegben (folyadékban) a kialakult egyensúlyi sebességgel süllyedő golyó sebességének megmérésével
- Az ekviprtíció tétele alapján: felfüggesztett piciny tükör forgási szabadsági fokán lévő \(\displaystyle \frac{1}{2}kT\) átlagos forgási energia megmérése a tükör véletlenszerű elfordulásai alapján (ebből közvetlenül a $k$ Boltzmann-állandó mérhető, amiből az $R$ univerzális gázállandó ismeretében $1\%$ pontossággal kiadódik $N_{\mathrm{A}}$)
- közvetetten az $F$ Faraday-állandó és az $e$ elemi töltés pontos kimérésével
- az ég kék színéből: a frekvenciafüggő fényszóródást a sűrűségfluktuációk (statisztikus eredetű sűrűségingadozások) is befolyásolják, amik kifejezésében ott szerepel az $N_{\mathrm{A}}$
- legújabban és legpontosabban: nagyon nagy pontossággal állandó sugarú ${}^{28}\mathrm{Si}$ egykristály golyó tömegének valamint a kristály rácsállandójának (röntgendiffrakcióval történő) mérésével
Az Avogadro-törvény tudománytörténeti jelentősége
Egyetlen gázmolekula tömege rettenetesen kicsi (például egy oxigénmolekula tömege csupán \(5,3\cdot 10^{-26}\ \mathrm{kg}\)) , ezért a mérése nagy nehézségekbe ütközik (bár ma már nagy pontossággal megoldható). Az Avogadro-hipotézis elfogadásával azonban a különféle gázok molekulatömegei - legalábbis egymáshoz képest - könnyen mérhetőkké váltak már 19. századi műszerekkel is, hiszen csak azonos állapotú gázok tömegeit kellett megmérni, márpedig néhány liter gáz tömege már jól mérhető. Tehát az Avogadro-törvény segítségével könnyen megállapíthatjuk, hogy az oxigéngáz molekulái kb. 16-szor nehezebbek, mint a hidrogéngáz molekulái. A gázok relatív molekulatömegeinek ilyetén meghatározása lendített a kémia tudományán. Másrészt a molekula és az atom fogalmainak szétválásához is hozzájárult az Avogadro-hipotézis, vagyis az atomelmélet egyik mérföldkövének tekinthető.
Az Avogadro-törvény felfedezésének története és utóélete
1809-ben Gay-Lussac publikálta új vizsgálatai eredményét. Ebben maradéktalanul lezajló kémiai reakciókat vizsgált, amikben a reagensek és/vagy a végtermékek közül legalább kettő gázhalmazállapotú volt. Gay-Lussac újítása abban állt, hogy a reagenseknek és végtermékeknek nemcsak a tömegarányait figyelte (ahogy akkoriban sokan), hanem a gázhalmazállapotúak szereplőknek a térfogatait is megvizsgálta; természetesen a korrekt összehasonlítás kedvéért a gáztérfogatokat azonos nyomáson és hőmérsékleten mérte. Azt kapta, hogy a gáztérfogatok arányai mindig kis egész számok (például \(1:1\) vagy \(1:2\) stb). Avogadro pedig Gay-Lussac ezen eredményei alapján állította fel hipotézisét.
Avogadro hipotézisét a publikálása után közel 50 éven át nem fogadták el. A tudomány fejlődése során gyakori, hogy egy korát megelőző felismerést (mint mozaik darabkát) amiatt nem fogadnak el, mert nincs még meg hozzá a kép, amibe "bele illene", nincs egy elmélet, ami alapján értelmezni lehetne az állítást, ezért inkább nem fogadják el az előremutató gondolatot. A tudományos közösség csak Avogadro halála (1856) után, 1858-ban fogadta el, amikor Stanislao Cannizzaro olasz professzor elméleti keretet adott hozzá. Avogadro ma a tudománytörténet nagy alakjának számít, de ez a 19. század első felében nagyon nem volt így.

Az Avogadro-számot nem sikerült Avogadro életében még megbecsülni sem. Az első ez irányú eredményes lépés az volt, hogy Loschmidt 1865-ben a kinetikus gázelméleti megfontolások segítségével nagyságrendileg helyesen kiszámolta az oxigéngáz molekuláinak átmérőjét, amire \(1\ \mathrm{nm}\)-t kapott. Ebből már meg lehetett becsülni az $1\ \mathrm{cm^3}$ térfogatnyi gázban lévő molekulák számát, amiből aztán az Avogadro-számot, de ezt csak 1873-ban Boltzmann számolta ki végül, és ő nevezte, méghozzá Loschmidt-számnak. Egészen a 20. század elejéig így nevezik az Avogadro-számot. Jean Perrin francia fizikus javasolta elsőként az Avogadro-konstans elnevezést 1909-ben, aki a 20. század elején több különböző módszerrel megmérte az Avogadro-állandót, amiért 1926-ban fizikai Nobel-díjat kapott. A 2019-től érvényes rendszerben az Avogadro-állandót az aktuálisan elérhető legpontosabb mérésekből adódó értéken rögzítették.